


GMPه¯¹و°´é’ˆه‰‚çڑ„ç”ںن؛§çژ¯ه¢ƒè¦پو±‚ه¦‚ن¸‹ï¼ڑ
(1)称é‡ڈو³¨و„ڈه‰©ن½™çڑ„هژںè¾…و–™ه؛”ه°پهڈ£è´®هکم€‚
(2)é…چهˆ¶هڈٹè؟‡و»¤è¦پهŒ؛هˆ†èƒ½وœ€ç»ˆçپèڈŒه’Œéوœ€ç»ˆçپèڈŒï¼Œç¨€é…چه’Œوµ“é…چ,é…چهˆ¶و—¶ç”¨ه¯†é—ç³»ç»ںè؟کوک¯éه¯†é—ç³»ç»ں,هگژ者ه¯¹çژ¯ه¢ƒçڑ„è¦پو±‚ه‡و¯”ه‰چ者é«کن¸€ن¸ھو،£و¬،ï¼›و›¾è¦پو±‚ن½؟用çڑ„و³¨ه°„用و°´هœ¨80℃ن»¥ن¸ٹن؟و¸©ن¸‹ه…¶è´®هکو—¶é—´ن¸چه®œè¶…è؟‡12 h,ن½†و–°GMPوŒ‡ه‡؛“و³¨ه°„用وœ¯هڈ¯é‡‡ç”¨70℃ن»¥ن¸ٹن؟و¸©ه¾ھçژ¯ï¼Œâ€ç›´وژ¥ن¸ژèچ¯و¶²وژ¥è§¦çڑ„وƒ°و€§و°”ن½“,ن½؟用ه‰چ需ç»ڈه‡€هŒ–ه¤„çگ†ï¼Œè¾¾هˆ°è§„ه®ڑçڑ„و´په‡€ه؛¦è¦پو±‚م€‚能وœ€ç»ˆçپèڈŒçڑ„è؟‡و»¤çژ¯ه¢ƒè‡³ه°‘وک¯Dç؛§ï¼Œè€Œé«کé£ژ险ن؛§ه“پçڑ„è؟‡و»¤çژ¯ه¢ƒه؛”ن¸؛cç؛§èƒŒو™¯ن¸‹çڑ„Aç؛§ï¼›éوœ€ç»ˆçپèڈŒهڈˆهڈ¯é™¤èڈŒè؟‡و»¤çڑ„è؟‡و»¤çژ¯ه¢ƒçڑ„è¦پو±‚ن¸؛cç؛§ï¼Œن¸چ能除èڈŒè؟‡و»¤çڑ„ن¸؛Bç؛§م€‚و–°GMPن¸ن¸چهˆ†ç²—م€پç²¾و»¤è€Œهگˆç§°è؟‡و»¤م€‚ن¹ںوœ‰وٹٹè؟‡و»¤ه’ŒçپŒه°پهگˆç§°é…چهˆ¶م€‚
(3)ه®‰ç“؟هˆ‡ه‰²ن¸ژهœ†هڈ£
(4)و´—ç“؟ه’ŒçپèڈŒè¦پو³¨و„ڈçژ»ç’ƒه®¹ه™¨هœ¨çپèڈŒه‰چè¦پè؟›è،Œن¸€ç³»هˆ—çڑ„و´—و¶¤ه’Œه¾ھçژ¯و·‹و´—,è؟™ه¯¹هژ»é™¤ç¢ژه±‘وک¯é‡چè¦پçڑ„,终و´—و°´è¦پ采用و³¨ه°„用و°´ï¼›è¦پو³¨و„ڈو´—هگژçڑ„ه¹²ç‡¥çپèڈŒم€په†·هچ´ه’Œو¸…و´پè´®هک,贮هک超è؟‡ن¸¤ه¤©è€…è¦پé‡چو–°و´—و¶¤م€پçپèڈŒï¼›ه¹²ç‡¥هگژوœ‰و•£çƒé—®é¢کم€‚
(5)çپŒه°پçپŒه°پوک¯ه°†و— èڈŒè؟‡و»¤هگژçڑ„ن؛§ه“پ装ه…¥و¸…و´—è؟‡è€Œن¸چهگ«çƒهژںçڑ„و— èڈŒه®¹ه™¨ن¸ه¹¶ه°پهڈ£çڑ„ه·¥è‰؛و¥éھ¤م€‚
çپŒه°پوک¯و•´ن¸ھو— èڈŒه·¥è‰؛ن¸çڑ„ه…³é”®ه·¥ه؛ڈم€په…³é”®و“چن½œï¼Œه› ن¸؛ه®ƒوک¯و— èڈŒè؟‡و»¤ن¹‹هگژه”¯ن¸€ن؛§ه“پوڑ´éœ²هœ¨ه¼€و”¾ç©؛و°”çژ¯ه¢ƒن¸çڑ„و“چن½œم€‚
و“چن½œè؟‡ç¨‹ن¸ه¦‚وœوœ‰ç›´وژ¥ن¸ژèچ¯و¶²وژ¥è§¦çڑ„وƒ°و€§و°”ن½“وˆ–هژ‹ç¼©ç©؛و°”,هˆ™è؟™ن؛›و°”ن½“ه؟…é،»è¾¾هˆ°ن¸€ه®ڑçڑ„و´په‡€و ‡ه‡†م€‚
ه؟…é،»ه¼؛è°ƒçپŒه°پçڑ„ه±€éƒ¨çژ¯ه¢ƒه؛”وک¯é‡چ点ن؟وٹ¤çڑ„ه…³é”®هŒ؛هںں,éوœ€ç»ˆçپèڈŒو³¨ه°„çپŒه°پè¦پو±‚وœ€é«کن¸€ç؛§çڑ„و´په‡€ه؛¦م€‚
هگ¹çپŒه°پ( BFS)وٹ€وœ¯هˆ™وک¯çپŒه°په·¥è‰؛çڑ„و–°هڈ‘ه±•م€‚ن¸؛ن؛†éپ؟ه…چçژ»ç’ƒه®¹ه™¨ه¤„çگ†ن¸ٹçڑ„é؛»çƒ¦ï¼Œé‡‡ç”¨ه،‘و–™çڑ„هگ¹çپŒه°پو—¥è¶‹و™®éپچم€‚هگ¹çپŒه°پç³»ç»ںوک¯ن¸€ه¥—ن¸“用وœ؛و¢°è®¾ه¤‡ï¼Œهڈ¯è؟ç»و“چن½œم€‚ه®ƒن½؟ه،‘و–™è¢‹çڑ„هˆ¶è¢‹ï¼ˆهگ¹و°”هˆ¶è¢‹هچ³ه°†çƒه،‘و€§وگو–™هگ¹هˆ¶وˆگه®¹ه™¨ï¼‰â€”—çپŒè£…——ه°پهڈ£ن¸‰è€…èپ”ن¸؛ن¸€ن½“م€‚و•´ن¸ھè؟‡ç¨‹ç”±ن¸€هڈ°ه…¨è‡ھهٹ¨وœ؛ه™¨ه®Œوˆگم€‚
GMPè¦پو±‚用ن؛ژç”ںن؛§éوœ€ç»ˆçپèڈŒن؛§ه“پçڑ„هگ¹çپŒه°پ设ه¤‡وœ¬è؛«ه؛”装وœ‰Aç؛§ç©؛و°”é£ژو·‹è£…置,هœ¨و“چن½œن؛؛ه‘کوŒ‰A/Bç؛§è¦پو±‚ç€è£…çڑ„و،ن»¶ن¸‹ï¼Œè¯¥è®¾ه¤‡هڈ¯ه®‰è£…هœ¨و´په‡€ه؛¦è‡³ه°‘ن¸؛Cç؛§çڑ„çژ¯ه¢ƒن¸م€‚
GMPè¦پو±‚用ن؛ژç”ںن؛§وœ€ç»ˆçپèڈŒçڑ„هگ¹çپŒه°پ设ه¤‡è‡³ه°‘ه؛”ه®‰è£…هœ¨Dç؛§çژ¯ه¢ƒن¸م€‚ 鉴ن؛ژهگ¹çپŒه°پوٹ€وœ¯çڑ„特و®ٹو€§ï¼Œهœ¨ه؛”用该وٹ€وœ¯و—¶ï¼ŒGMPه¼؛è°ƒè¦پو³¨و„ڈن»¥ن¸‹هگ„点ï¼ڑ
设ه¤‡çڑ„设è®،ه’ŒéھŒè¯پï¼›
设ه¤‡هœ¨ç؛؟وƒ…ه†µه’Œهœ¨ç؛؟çپèڈŒçڑ„éھŒè¯پهڈٹ结وœçڑ„é‡چçژ°و€§ï¼›
设ه¤‡و‰€ه¤„çڑ„و´په‡€هŒ؛çژ¯ه¢ƒï¼›
设ه¤‡و“چن½œن؛؛ه‘کçڑ„هں¹è®ه’Œç€è£…ï¼›
设ه¤‡ه…³é”®هŒ؛هںںه†…çڑ„و“چن½œï¼ŒهŒ…و‹¬çپŒه°په¼€ه§‹ه‰چ设ه¤‡çڑ„و— èڈŒè£…é…چم€‚
(6)éڑ”离و“چن½œوٹ€وœ¯هœ¨ن¸ٹن¸–ç؛ھ80ه¹´ن»£ه‡؛çژ°ن؛ژهچٹه¯¼ن½“ه’Œه¾®ç”µهگ领هںںçڑ„éڑ”离ه™¨وٹ€وœ¯ï¼Œçژ°ه·²وˆگن¸؛و— èڈŒهˆ¶èچ¯و–¹é¢çڑ„ه…ˆè؟›وٹ€وœ¯م€‚GMP规ه®ڑ“é«کو±،وں“é£ژ险çڑ„و“چن½œه®œهœ¨éڑ”离ه™¨ن¸ه®Œوˆگâ€م€‚éڑ”离ه™¨çڑ„“ن¼ 输装置هڈ¯è®¾è®،وˆگهچ•é—¨وˆ–هڈŒé—¨م€پç”ڑ至هڈ¯ن»¥وک¯هگŒçپèڈŒè®¾ه¤‡ç›¸è؟çڑ„ه…¨ه¯†ه°پç³»ç»ںâ€م€‚GMP规ه®ڑهڈھوœ‰ç»ڈè؟‡é€‚ه½“çڑ„éھŒè¯پ,éڑ”离ه™¨و–¹هڈ¯وٹ•ه…¥ن½؟用م€‚
(7)çپèڈŒه¯¹ن؛ژ能وœ€ç»ˆçپèڈŒçڑ„é’ˆه‰‚ن¸€èˆ¬ç”¨هڈŒو‰‰ه¼ڈçپèڈŒوںœï¼ŒçپèڈŒوںœه؛”ه®ڑوœںè؟›è،Œه†چéھŒè¯پï¼›çپŒه°پن¸ژçپèڈŒçڑ„و—¶é—´é—´éڑ”و„ˆçںو„ˆه¥½ï¼Œن¸€èˆ¬ن¸چ超è؟‡4hم€‚
(8)و£€و¼ڈçپèڈŒهگژه؟…é،»و£€و¼ڈ,وŒ‘ه‡؛ه°پهڈ£ن¸چن¸¥çڑ„هچٹوˆگه“پم€‚
(9)çپ¯و£€وŒ‰م€ٹو¾„وکژه؛¦و£€وں¥ç»†هˆ™ه’Œهˆ¤و–و ‡ه‡†م€‹و£€وں¥و¾„وکژه؛¦م€‚
(10)هŒ…装(هŒ…و‹¬هچ°ه—م€پè´´ç¾ï¼‰م€‚
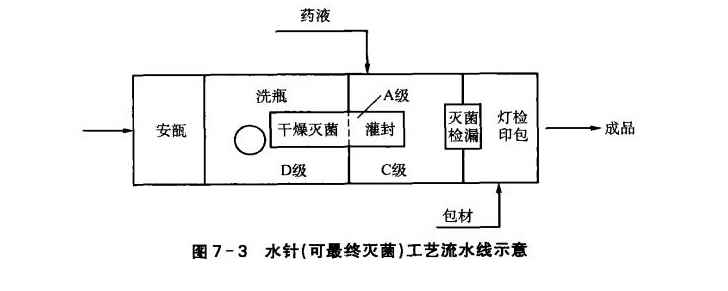
ه›¾7 3ن¸؛و°´é’ˆه·¥è‰؛وµپو°´ç؛؟çڑ„ç¤؛و„ڈم€‚
وœ¬و–‡و ‡ç¾ï¼ڑGMP
هœ°ه€ï¼ڑه±±ن¸œçœپوµژهچ—ه¸‚ه¤©و،¥هŒ؛و–°ه¾گه±…ه§”ن¼ڑ黄و²³ه»؛邦ه¤§و،¥è¥؟ن¾§1-6هڈ· 电è¯ï¼ڑ0531-68824415 ن¼ çœںï¼ڑ0531-68824415
版وƒو‰€وœ‰:وµژهچ—é،؛ه¥‡ه‡€هŒ–ه·¥ç¨‹وœ‰é™گه…¬هڈ¸ وٹ€وœ¯و”¯وŒپï¼ڑه؛·ç¾ژ科وٹ€ ه¤‡و،ˆهڈ·:é²پICPه¤‡19040779هڈ· xmlهœ°ه›¾ htmlهœ°ه›¾ txtهœ°ه›¾ ç™»ه½•